Quotidiano on line
di informazione sanitaria
Giovedì 25 APRILE 2024
Scienza e Farmacidi informazione sanitaria
Giovedì 25 APRILE 2024
Sperimentazioni cliniche. Nel 2015 ne sono state autorizzate 672. Al top quelle in oncologia e sulle malattie rare. Il rapporto Aifa
Rispetto al 2014 incremento del 13,5% in termini assoluti delle sperimentazioni autorizzate ma rispetto all’anno scorso cala leggermente la percentuale di sperimentazioni made in Italy sul totale di quelle europee. Per il 45,5% si tratta di sperimentazioni di fase III. IL RAPPORTO AIFA
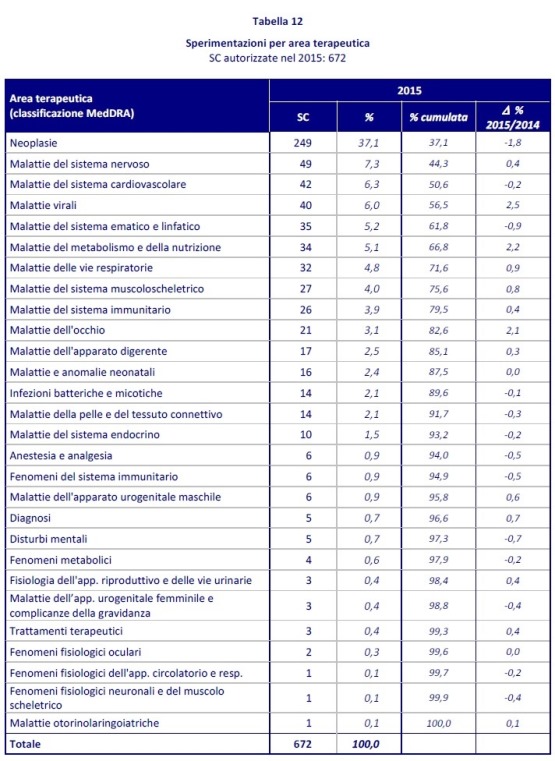
04 GEN - L’Agenzia Italiana del Farmaco ha pubblicato il 15° Rapporto Nazionale sulla Sperimentazione Clinica dei medicinali in Italia con i dati relativi al 2015. Su un totale di 672 sperimentazioni autorizzate nell’anno, il 37% (249) in oncologia e il 24,9% (167) per le malattie rare.Rispetto all’anno precedente, sottolinea Aifa, “si rileva una sostanziale stabilità del numero di sperimentazioni cliniche condotte nel nostro Paese che rende necessaria una costante attenzione da dedicare a questo settore per far raggiungere all’Italia il livello di competitività auspicato nel contesto europeo”.
Se infatti il numero di sperimentazioni cliniche autorizzate è aumentato passando dalle 592 del 2014 alle 672 del 2015, il confronto con gli altri paesi dell’Unione Europea mostra un decremento delle sperimentazioni made in Italy che passano dal 18,2% al 17,2% del totale.
Durante l’anno 2014, si legge nel rapporto, si era visto un potenziale trend in aumento delle sperimentazioni cliniche in Italia che aveva portato a ipotizzare un futuro di primo piano nel settore delle sperimentazioni cliniche.
Tuttavia, prosegue il rapporto Aifa, il dato del 2015 ha rilevato una sostanziale stabilità rispetto al quadro europeo ricordandoci, pertanto, la necessaria attenzione da dover dedicare a questo settore per far raggiungere all’Italia il livello di competitività auspicato.
Da un esame generale, infatti, emerge che i dati del 2015 relativi alla distribuzione delle sperimentazioni cliniche per fascia, ATC e classe terapeutica, popolazione coinvolta, disegno sperimentale, Promotore profit o no profit, non si discostano in maniera significativa da quelli del 2014.
Inoltre, sottolinea il rapporto, poiché il numero di richieste di valutazione di sperimentazioni cliniche non è corrisposto a quello delle sperimentazioni cliniche valutate a causa del naturale prolungamento del processo di valutazione e autorizzazione dall’anno precedente a quello successivo, l’elaborazione statistica dei dati si è concentrata sul totale delle sperimentazioni concluse nell’anno 2015.
In numero assoluto, vi è stato un lieve aumento nel numero globale di sperimentazioni profit. E’ continuato il trend in aumento delle sperimentazioni su farmaci biologici/biotecnologici (32,8% includendo i farmaci di combinazione) e su farmaci di terapia avanzata (passati dal 2% al 2,7%) che mostra, tuttavia, una crescita meno esponenziale rispetto ai dati valutati per la prima metà del 2015.
Si conferma il primato assoluto delle sperimentazioni in oncologia(249 su 672 totali) che presentano, per la prima volta in tanti anni, una lieve flessione (-1,8%) come percentuale sulle sperimentazioni totali.
La distribuzione delle sperimentazioni per fase si mantiene nelle stesse proporzioni rispetto agli anni precedenti, con una buona rappresentatività delle sperimentazioni di fase I e I/II e un lieve aumento delle sperimentazioni di fase II. In tutto sono state 69 quelle di fase I, 224 quelle di fase II, 306 in fase III, 68 in fase IV e 5 quelle per bioequivalenza e biodisponibilità.
Le sperimentazioni nelle malattie rare continuano ad aumentare, anche se di poco, rispetto all’anno precedente. In tutto sono state autorizzate 167 sperimentazioni per malattie rare pari al 24,9% del totale con un ulteriore aumento delle sperimentazioni profit e delle sperimentazioni in fase più avanzata di sviluppo: questo segnale riflette l’evoluzione progressiva che sta vivendo lo scenario farmacologico attuale e che si intravede per il prossimo futuro, con l’arrivo in quantità crescente di farmaci innovativi e di risposte terapeutiche per patologie attualmente ancora prive di cura.
Il dato relativo alle sperimentazioni nella popolazione pediatrica e nella popolazione femminile, il cui numero costantemente basso ormai da anni si è riconfermato al ribasso anche nel 2015, ha rappresentato nel 2016 un elemento a supporto della scelta delle aree tematiche per il Bando AIFA sulla Ricerca Indipendente.
04 gennaio 2017
© Riproduzione riservata
Allegati:
Altri articoli in Scienza e Farmaci
gli speciali
Quotidianosanità.it
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Direttore responsabile
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Tel. (+39) 06.89.27.28.41
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
- Joint Venture
- SICS srl
- Edizioni
Health Communication srl
Copyright 2013 © QS Edizioni srl. Tutti i diritti sono riservati
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy