Quotidiano on line
di informazione sanitaria
Martedì 23 APRILE 2024
Scienza e Farmacidi informazione sanitaria
Martedì 23 APRILE 2024
Sperimentazioni cliniche. Crescono quelle presentate in Italia. Ma le “nazionali” sono sempre meno. Il nuovo Rapporto Aifa
La distribuzione delle sperimentazioni per area terapeutica conferma il dato degli anni precedenti, con circa la metà in ambito oncologico ed emato-oncologico. Continua in maniera significativa il trend in rialzo dei trial in malattie rare, che rappresentano il 32,1% del totale (31,5% nel 2018). Scendono le sperimentazioni no profit. IL REPORT
31 DIC - Le sperimentazioni cliniche presentate in Italia nel 2019 (672), dopo il calo del 2017 (564), si sono mantenute sui livelli storici recuperati già a partire dal 2018 (666) come numero totale, pur in un contesto di contrazione costante e generale delle sperimentazioni condotte in Europa. Ciò ha portato a un ulteriore incremento della percentuale di sperimentazioni autorizzate in Italia rispetto al resto d’Europa (pari al 22%). È quanto contenuto nel 19° Rapporto nazionale di Aifa sulla Sperimentazione Clinica dei medicinali in Italia, con i dati relativi al 2019.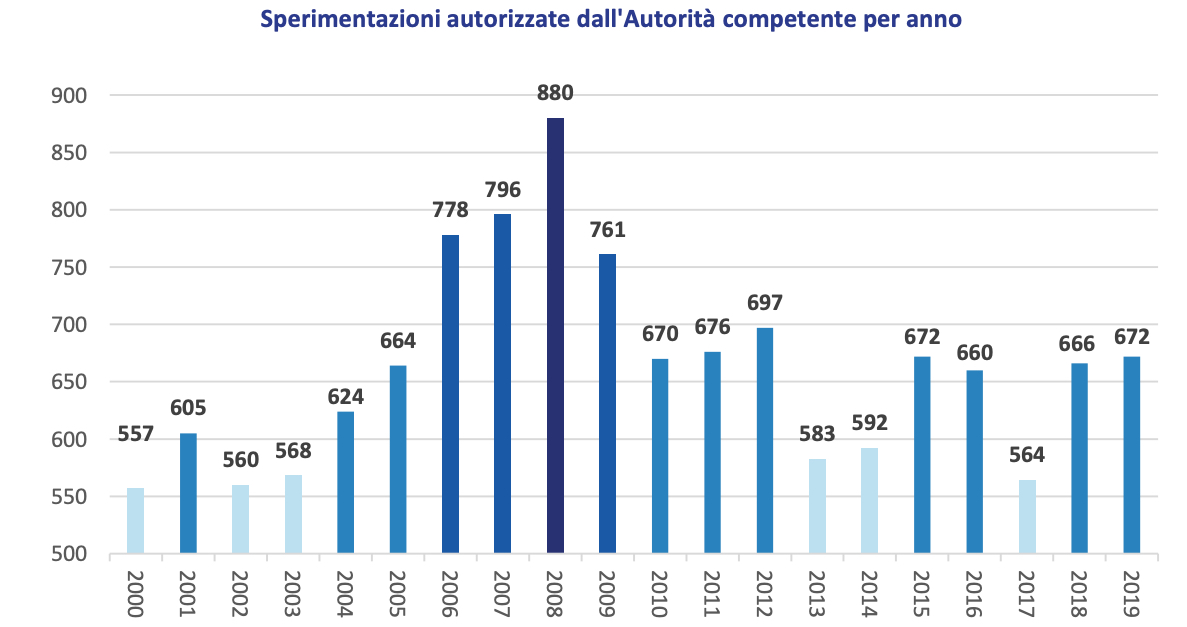
Una delle differenze principali rispetto all’anno precedente è l’inversione di tendenza delle sperimentazioni puramente nazionali, con una contrazione rispetto alle sperimentazioni internazionali, che invece sono aumentate anche in numero assoluto, confermando come in Italia le sperimentazioni multicentriche e multinazionali siano la tipologia prevalente. Come già detto, nel 2019 sono state autorizzate in Italia 672 sperimentazioni cliniche: di queste 543 (80,8%) sono internazionali (506, 76% nel 2018) e 129 (19,2%) nazionali (160, 24% nel 2018). Le 129 sperimentazioni nazionali sono ripartite quasi a metà tra monocentriche e multicentriche, 62 e 67 rispettivamente, mentre le 543 internazionali sono suddivise in 473 multicentriche (35 condotte in UE e 438 anche con il coinvolgimento di Paesi extra UE, rappresentando la tipologia più consistente) e 70 monocentriche (di cui solo 18 riguardanti esclusivamente Paesi UE). Il dato globale sulla ripartizione tra nazionali e internazionali delle sperimentazioni autorizzate in Italia nel 2019 è pari a 80,8% versus 19,2% e non si discosta significativamente dai dati degli anni precedenti
La distribuzione delle sperimentazioni per area terapeutica conferma il dato degli anni precedenti, con circa la metà in ambito oncologico ed emato-oncologico.
Continua in maniera significativa il trend in rialzo dei trial in malattie rare, che rappresentano il 32,1% del totale (31,5% nel 2018), di cui quasi l’82% sperimentazioni profit, con una distribuzione prevalente nelle fasi II e III di sperimentazione. Le sperimentazioni su malattie rare di fase I rappresentano tuttavia il 39% di tutte le sperimentazioni di fase I autorizzate in Italia nel 2019.
Un altro dato in leggera controtendenza rispetto all’anno precedente riguarda le sperimentazioni no profit che, rispetto al totale di quelle condotte in Italia, si attestano al 23,2% rispetto al 27,3% registrato nel 2018.
Il dato relativo alle sperimentazioni pediatriche torna invece ai livelli degli anni precedenti, attestandosi al 9,1% rispetto all’11,4% del 2018.
Il Rapporto contiene anche in questa edizione i dati relativi alla partecipazione dell’Italia al progetto Voluntary Harmonisation Procedure (VHP) per la valutazione congiunta dei protocolli clinici che si svolgono in più Stati dell’Unione Europea.
Anche nel 2019 l’Italia è stato uno dei principali Stati membri a gestire le VHP, con 25 sperimentazioni su 115 e 128 emendamenti sostanziali gestiti come Reference Member State. In continuo incremento è anche il numero delle VHP valutate in maniera coordinata con il rispettivo Comitato etico.
Questa edizione del Rapporto presenta una eccezione rispetto agli anni precedenti, in virtù del periodo eccezionale che la sanità pubblica e le sperimentazioni cliniche hanno attraversato e stanno ancora attraversando per la pandemia da COVID-19. Sono stati quindi inseriti i dati preliminari relativi alle sperimentazioni cliniche su farmaci per il trattamento del COVID-19, limitatamente al periodo marzo-settembre. In generale sono state autorizzate 44 sperimentazioni.
31 dicembre 2020
© Riproduzione riservata
Altri articoli in Scienza e Farmaci
gli speciali
Quotidianosanità.it
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Direttore responsabile
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Tel. (+39) 06.89.27.28.41
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
- Joint Venture
- SICS srl
- Edizioni
Health Communication srl
Copyright 2013 © QS Edizioni srl. Tutti i diritti sono riservati
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy