di informazione sanitaria
Sabato 04 MAGGIO 2024
Dispositivi personalizzati per il paziente: il ruolo della tecnologia 3D nella produzione di device impiantabili.
di Aurelio Secinaro, Luca BorroLa tecnologia 3D è uno degli strumenti che più di altri permette di perseguire l’obiettivo di dare al paziente una cura personalizzata e consente di produrre una varietà di dispositivi biomedici perfettamente customizzati.
08 FEB - Dalla biologia alla bioingengeria fino alla medicina negli ultimi 10 anni si sta verificando una tendenza molto chiara da parte della scienza medica ad orientare le attività cliniche di cura verso la cosiddetta medicina personalizzata. Si tratta di un approccio fondato sulla personalizzazione delle cure in base alle caratteristiche fisiologiche del paziente. Le cure che oggi vengono offerte in molti centri clinici avanzati tendono ad essere customizzate sul paziente, sulle sue caratteristiche biologiche, genetiche, fisiche e morfometriche. Sebbene questo approccio non sia ancora generalizzato e ampiamente diffuso ci si sta sempre di più allontanando alla “generalità della cura” e sempre più orientando all’attenzione massima alla personalizzazione del trattamento per ogni specifico paziente.Già l’oncologia medica si sta indirizzando verso questo tipo di approccio clinico e l’epigenomica, la branca della genetica che studia le interazioni tra DNA e ambiente, è un filone di ricerca di grande interesse che consente di considerare non solo l’individuo come insieme di cellule e geni ma anche come tali cellule e geni vengono condizionati dall’ambiente con cui l’individuo interagisce.
La tecnologia 3D è probabilmente uno degli strumenti che più di altri permette di perseguire l’obiettivo di dare al paziente una cura personalizzata. Questo perché la possibilità di ottenere oggetti biologici tridimensionali o dispositivi biomedici personalizzati si rende possibile anche soprattutto grazie a tecnologie innovative in grado di realizzare tali prodotti con relativa semplicità.
Possiamo dividere l’uso del 3D nella medicina personalizzata in due grandi macro-categorie: la prima che riguarda la concreta applicabilità clinica del 3D nell’ambito di numerose specialità mediche quali la chirurgia maxillo facciale, l’ortopedia, l’odontoiatria, la neurochirurgia. La seconda invece riguarda principalmente il versante della ricerca biomedica attraverso l’uso del 3D Bioprinting, una tecnica di stampa 3D di materiale biologico (anche autologo) che consente di ricreare in vitro forme e geometrie paziente specifiche con materiale cellulare proveniente dal paziente stesso. Di quest’ultima possibilità tecnologica parleremo nei altri articoli su questa testata.
LA STAMPA 3D DI BIOMATERIALI PER LA MEDICINA PERSONALIZZATA
La stampa 3D oggi consente di produrre una varietà di dispositivi biomedici perfettamente customizzati sul paziente. Questo consente di offrire un più alto livello di cura, una minore incidenza di complicanze intra e post-operatorie e una migliore compliance del paziente al trattamento chirurgico ricevuto.
La grande svolta in questo senso non arriva propriamente dalla stampa 3D ma dalla disponibilità di materiali biocompatibili innovativi in grado di poter essere stampati in 3D per produrre così dispositivi medici paziente-specifici. Generalmente si tratta di:
-
Protesi per uso ortopedico: in particolare protesi di anca, ginocchio, gomito, spalla.
Sono generalmente protesi stampate in 3D in leghe metalliche (ad es. titanio) e spesso combinate con materiali di diversa natura quali quelli bioceramici. - Protesi per uso chirurgico maxillo-facciale: si tratta di protesi generalmente in titanio oppure in materiali bioriassorbibili quali i poliesteri. Nell’ambito della chirurgia maxillo facciale è molto sviluppato l’utilizzo di placche di osteosintesi stampate in 3D sulla base di una preventiva ricostruzione 3D dell’anatomia ossea del paziente.
-
Protesi per uso Odontoiatrico: si tratta della stampa 3D di denti provvisori in resine biocompatibili oppure di membrane di osteorigenerazione stampate in tecnopolimeri biocompatibili come il PET.
L’odontoiatria inoltre si avvale della stampa 3D anche per la produzione di dispositivi utilizzati come ausilio temporaneo alla chirurgia quali le dime chirurgiche anch’esse stampate in materiali resinici biocompatibili. - Protesi per Neurochirurgia: in questo ambito specialistico il principale utilizzo della tecnologia di produzione additiva è quello relativo alla produzione di placche di osteosintesi e sostituti biocompatibili per la ricostruzione della teca cranica. Si usano normalmente leghe metalliche e materiali bioceramici come l’idrossiapatite, uno dei minerali maggiormente contenuti nella matrice ossea.
A prescindere dall’ambito di applicazione la produzione additiva di dispositivi medici impiantabili è preceduta da un attento lavoro di ricostruzione anatomica 3D della parte anatomica interessata dall’impianto. Questo lavoro è generalmente eseguito tramite software specializzati e personale addestrato. La ricostruzione 3D anatomica ottenuta da immagini TAC o RMN deve poi essere seguita dal disegno CAD (Computer Aided Design) del dispositivo biomedico che si intende stampare e impiantare. La progettazione di tale dispositivo deve seguire una serie di importanti regole derivate principalmente dall’ingegneria biomedica.
In questo contesto di progetto assumono grande importanza lo studio della forma, degli spessori, dei punti di criticità meccanica e di tutti quei fattori che condizionano sia la stampabilità dell’oggetto sia la sua resistenza meccanica una volta sottoposto a stress meccanici di esercizio.
Generalmente il processo di progettazione 3D di un dispositivo biomedico paziente-specifico è interessato anche da una fase di analisi e test del progetto attraverso la FEA (Finite Element Analysis), una procedura ingegneristica di analisi meccanica che permette di prevedere il comportamento fisico-meccanico del dispositivo ancora prima della sua produzione e del suo impianto. L’interpretazione dei risultati dei test agli elementi finiti consente all’ingegnere di apportare modifiche al progetto work in progress al fine di renderlo compatibile con gli obiettivi finali desiderati.
La stampa 3D di dispositivi biomedici, attività ormai in uso nella routine clinica di un consistente numero di centri ospedalieri maggiori in tutto il mondo (compresa l’Italia), è un’attività che richiede un certo livello di controllo della qualità oltre che strumentazioni all’avanguardia non proprio facili da gestire.
I biomateriali più utilizzati per la produzione di questi dispositivi medici personalizzati sono i materiali metallici (soprattutto titanio), bioceramiche e biopolimeri.
Materiali Metallici: generalmente sono gli acciai inossidabili, il cromo-cobalto e il titanio. Quest’ultimo è largamente utilizzato per la sua notevole biocompatibilità e la sua alta resistenza alla corrosione. Essendo infatti i materiali metallici tutti soggetti a ossidazione da parte dell’ambiente fisiologico ricco di ossigeno la resistenza a corrosione è una delle qualità che si richiede ad un materiale metallico da usare per la produzione di un dispositivo biomedico. Vengono generalmente impiegati per l’utilizzo nell’ambito dell’ortopedia, chirurgia maxillo facciale e odontoiatria dove è necessario avere materiali le cui caratteristiche meccaniche risultino simili a quelle del tessuto osseo. Le leghe di Titanio in effetti presentano un modulo elastico (cioè la tendenza del materiale a deformarsi quando sottoposto ad un certo carico) simile a quello dell’osso (dai 10 ai 40 GPa).
Materiali Bioceramici: sono molto utilizzati per la fabbricazione di dispositivi medici per via della loro resistenza alla corrosione (a differenza dei metallici), della loro lavorabilità, del loro basso attrito e della loro capacità ad integrarsi perfettamente con i tessuti biologici.
Tra i materiali ceramici più conosciuti ci sono sicuramente l’Allumina molto usata in ambito odontoiatrico e ortopedico, l’idrossiapatite, Calcio Fosfati e i biovetri.
L’allumina è definito come un bioceramico “inerte” ossia non in grado di attivare interazioni biologiche con i tessuti con i quali viene a contatto.
I calcio fosfati e biovetri invece sono considerati come materiali “bioattivi” ossia fortemente in grado di interagire (positivamente) con i tessuti biologici con i quali tali materiali scambiano stimoli chimico-fisici in grado di indurre la rigenerazione tissutale.
Biopolimeri: si tratta di polimeri generalmente appartenenti alla famiglia dei poliesteri aventi caratteristiche particolari di biocompatibilità e biodegradabilità. Vengono impiegati nella produzione di dispositivi biomedici soprattutto per la loro alta lavorabilità, per la loro facile reperibilità e per la possibilità di indurre fenomeni biologici controllati nei tessuti.
Tra i più utilizzati troviamo il PLA (Acido Polilattico) già usato per la produzione di stent cardiovascolari ma anche il PET e il PCL diffusamente usato nella produzione di fili di sutura.
La loro caratteristica peculiare è la riassorbibilità: tali polimeri infatti vengono riassorbiti da fenomeni fisici quali l’idrolisi dei legami estere presenti nella molecola.
Nonostante le interessanti prospettive che tali biomateriali hanno aperto nel settore biomedico fin dagli anni 60 si tratta comunque di tre categorie di materiali che richiedono infrastrutture tecniche complesse per la loro lavorazione. I primi due richiedono la stampa 3D a partire da polveri di materiale. Questa tipologia di stampa prevede l’uso di un laser che unisce particelle di materiale tramite un collante sintetico o tramite fusione delle particelle stesse. La strumentazione tecnica (stampanti 3D e Stazioni di Post-produzione) richiesta per questo tipo di stampa ha costi di molto superiori ai 100.000 euro e richiede spazi di lavoro adeguati. Generalmente questi spazi non possono essere previsti in un contesto ospedaliero ma sono di esclusiva pertinenza di strutture industriali e di aziende esterne che si occupano di produrre tali dispositivi per gli ospedali.
Nel caso dei tecnopolimeri invece è possibile ridimensionare l’infrastruttura tecnica richiesta per la loro stampa 3D al punto che potrebbero essere anche stampati all’interno delle strutture ospedaliere stesse a patto che si disponga però di macchinari adeguati, ossia di particolari tipologie di stampanti 3D aventi specifiche caratteristiche soprattutto in termini di mantenimento delle temperature di stampa oltre che spazi di lavoro idonei.
Indipendentemente dalla tipologia di materiale tuttavia è necessario che l’approvvigionamento degli stessi avvenga da fornitori in grado di garantire biocompatibilità dei materiali e un certo standard di qualità della materia prima.
È di fondamentale importanza poi considerare che i dispositivi medici ottenuti tramite stampa 3D possono avere delle caratteristiche meccaniche anche di molto diverse dai dispositivi ottenuti tramite processi produttivi tradizionali (stampaggio, ad esempio). Questo perché la stampa 3D produce oggetti strato dopo strato creando così una condizione meccanica dell’oggetto che va attentamente valutata da personale qualificato. Questo è vero soprattutto quando si parla di “sterilizzazione” dei dispositivi medici stampati in 3D. Soprattutto quando si tratta di dispositivi medici stampati in termopolimero (PLA, PET) è necessario studiare qual è il metodo di sterilizzazione più adatto e sicuro sia dal punto di vista di abbattimento di contaminanti nel dispositivo sia dal punto di vista dell’integrità post-sterilizzazione del dispositivo medico stampato. In tal caso le temperature e il tempo di sterilizzazione giocano un ruolo determinante nel mantenimento dell’integrità strutturale dei dispositivi medici ottenuti tramite additive manufacturing.
Il grande interesse scientifico degli ultimi 10 anni si è concentrato sui materiali bioattivi quelli, cioè, in grado di attivare delle relazioni biologiche con i tessuti con i quali vengono impiantati. In sostanza questi materiali sono quelli che stanno lentamente trasformando la stampa 3D in stampa 4D dove la quarta dimensione è costituita proprio dal “tempo”. E’ proprio la capacità di tali materiali di modificarsi con il tempo all’interno dell’organismo umano che li rende interessanti da applicare in medicina.
Si pensi ad esempio alla chirurgia pediatrica dove dispositivi biomedici inerti che non seguono le fasi di crescita del bambino possono costituire una soluzione tecnologica solo per un certo periodo di tempo, richiedendo nel tempo una revisione chirurgica con la possibilità di dover sostituire l’impianto per adeguarlo alla crescita del soggetto.
Con i biomateriali, grazie alla loro bioriassorbibilità, si apre uno scenario diverso e maggiormente orientato all’integrazione di tali materiali con la natura biologica dei processi fisiologici di rigenerazione dei tessuti.
A tal proposito è utile presentare il primo impianto europeo di splint bronchiale bioriassorbibile stampato in 3D in un paziente pediatrico affetto da una grave forma di tracheobroncomalacia. L’intervento, il cui pioniere mondiale è il Prof. Glen Green dell’Università del Michigan, è stato condotto con successo dall’equipe chirurgica della Cardiochirurgia e della Chirurgia delle Vie Aeree dell’Ospedale Bambino Gesù di Roma nel 2019. A questo primo intervento sono seguiti poi altri 3 casi di impianto di splint bronchiale stampato in 3D, tutti portati a termine con successo.
L’obiettivo di uno splint bronchiale stampato in 3D è quello di superare tutte le criticità che si riscontrano con i sistemi tradizionali di trattamento delle tracheobroncomalacie. Parliamo ad esempio di sistemi di dilatazione ripetuta delle vie aeree che spesso danno origine a recidive della malattia oppure dell’impianto di stent metallici in pazienti pediatrici con enormi rischi in termini di “migrabilità” dello stent nelle vie aeree e del mancato adeguamento dello stent metallico alla crescita del paziente.
La tracheobroncomalacia severa in età pediatrica dunque è un esempio evidente di necessità clinica di impianto di un dispositivo medico paziente-specifico in grado di evolvere con il paziente negli anni senza creare problematiche di incongruenza biologica tra lo sviluppo fisiologico del contesto tracheobronchiale e lo stent stesso.
L’obiettivo che l’equipe chirurgica del Bambin Gesù si è posto, sulla scia di quanto già da anni realizzato in America su questo tema, è quello di realizzare tramite stampa 3D uno splint bronchiale personalizzato per il paziente e stampato in un biopolimero biocompatibile e biodegradabile quale il Policaprolattone unito ad una piccola parte di Idrossiapatite (un materiale bioceramico quasi completamente inerte). Questo composto di biopolimeri è in grado di rimanere in situ per circa 24 mesi fino a biodegradarsi in autonomia completamente per distruzione idrolitica dei legami estere del policaprolattone.
Lo splint è stato realizzato a partire da un’accurata indagine radiologica e dalla ricostruzione 3D del modello tracheo-bronchiale del paziente sul quale lo splint stesso è stato disegnato e dimensionato.
Successivamente il modello 3D dello splint è stato inviato alla stampa 3D in un centro di additive manufacturing dotato di strumentazione di stampa di tipo SLS (Selective Laser Sintering).
Il dispositivo biomedico è stato così impiantato secondo una procedura autorizzativa all’uso compassionevole vista la gravità della condizione clinica del paziente e l’assenza di alternative terapeutiche valide. Ogni dispositivo biomedico impiantato, com’è noto, causa delle reazioni immunitarie più o meno pronunciate. La reazione attesa dall’impianto di questo dispositivo di splintaggio bronchiale in biopolimero era quella della formazione di tessuto fibroso-cicatriziale perimplantare. Tale evenienza però oltre ad essere attesa, nel caso specifico, era anche voluta in quanto in grado di conferire una naturale rigidità strutturale al bronco una volta che il dispositivo si fosse riassorbito.
E’ stato così ripristinato il calibro bronchiale del paziente il quale quindi ha potuto sospendere definitivamente l’ossigenoterapia e riprendere una vita normale.
CONCLUSIONI
Una delle più importanti sfide odierne per migliorare le possibilità di trattamento di patologie complesse è rappresentata dalla massima personalizzazione delle cure. Questo è possibile anche, soprattutto, grazie all’uso delle nuove tecnologie applicabili al settore biomedicale quale la stampa 3D. Il vero problema di questo approccio però è solo in rarissimi casi costituito dalla disponibilità di tecnologie di stampa efficienti. Nella maggior parte dei casi infatti il problema è la ricerca di biomateriali in grado di integrarsi perfettamente nell’organismo umano senza generare risposte infiammatorie abnormi e in grado di raggiungere il giusto equilibrio tra biodegradazione del polimero e rigenerazione dei tessuti trattati.
Un delle prospettive più interessanti in tal senso è l’unione di biopolimeri sintetici (quali ad esempio il Policaprolattone) con biopolimeri naturali (quali ad esempio il collagene) per avvicinare sempre di più il dispositivo biomedico stampato in 3D all’ambiente biologico naturale in vivo.

Figura 1: Ricostruzione 3D dell'albero bronchiale del paziente con la rilevazione di misure relative al calibro bronchiale nelle diverse fasi espiratorie. Si può notare, nell'ultima immagine a destra, la riduzione notevole del calibro del bronco destro.

Figura 2: a sinistra e al centro il modello 3D dei bronchi del paziente con lo splint bronchiale realizzato secondo l'anatomia bronchiale. A destra il dettaglio del dispositivo realizzato al CAD.
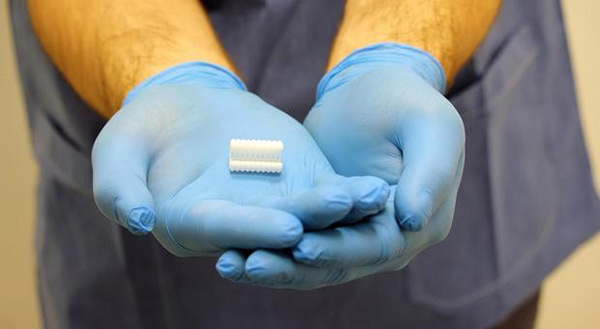
Figura 3: Lo splint bronchiale stampato in 3D.

Figura 4: serie di Splint bronchiali stampati in 3D in Policaprolattone e Idrossiapatite
Aurelio Secinaro, Responsabile Radiologia Toracica e Cardiovascolare Avanzata, Coordinatore del Laboratorio 3D, Ospedale Pediatrico Bambino Gesù, Roma
Luca Borro, Ingegnere Biomedico, Laboratorio 3D, Ospedale Pediatrico Bambino Gesù, Roma
08 febbraio 2022
© Riproduzione riservata
Allegati:
Altri articoli in Scienza e Farmaci
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
- Joint Venture
- SICS srl
- Edizioni
Health Communication srl
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy






