Quotidiano on line
di informazione sanitaria
Giovedì 02 MAGGIO 2024
Scienza e Farmacidi informazione sanitaria
Giovedì 02 MAGGIO 2024
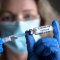
Vaccino Covid. Ema avvia una seconda valutazione dei dati sperimentali. Si tratta del vaccino sviluppato da BioNTech in collaborazione con Pfizer
Questo nuovo vaccino (BNT162b2) agisce preparando l'organismo a difendersi dall'infezione con il coronavirus SARS-CoV-2. Il virus utilizza proteine sulla sua superficie esterna, chiamate proteine spike, per entrare nelle cellule del corpo e causare malattie. BNT162b2 contiene le istruzioni genetiche (mRNA) per la proteina spike ed è ricoperto da piccoli grassi (particelle lipidiche) che impediscono la degradazione dell'mRNA.
06 OTT - Il comitato per i medicinali per l'uomo (CHMP) dell'EMA, dopo quella avviata nei giorni scorsi sul vaccino AstraZeneca, ha avviato una seconda "revisione continua" (rolling review) dei dati di un altro vaccino per COVID-19 noto come BNT162b2, sviluppato da BioNTech in collaborazione con Pfizer.L'avvio della revisione progressiva significa che il comitato ha iniziato a valutare il primo lotto di dati sul vaccino, che provengono da studi di laboratorio (dati non clinici). Ciò non significa che si possa ancora giungere a una conclusione sulla sicurezza e l'efficacia del vaccino, poiché gran parte delle prove deve ancora essere sottoposta al comitato.
La decisione del CHMP di avviare la revisione progressiva di BNT162b2 si basa sui risultati preliminari di studi clinici precoci e non clinici condotti su adulti che suggeriscono che il vaccino innesca la produzione di anticorpi e cellule T (cellule del sistema immunitario, difese) che prendono di mira il virus.
Sono in corso studi clinici su larga scala che coinvolgono diverse migliaia di persone e i risultati saranno disponibili solo nelle prossime settimane e mesi. Questi risultati forniranno informazioni sull'efficacia del vaccino nel proteggere le persone dal COVID-19 e saranno valutati non appena saranno disponibili. Verranno inoltre esaminati tutti i dati disponibili sulla sicurezza del vaccino e sulla sua qualità (come i suoi ingredienti e il modo in cui è prodotto).
EMA completerà la sua valutazione secondo i suoi standard usuali di qualità, sicurezza ed efficacia. Sebbene la tempistica complessiva della revisione non possa ancora essere prevista, il processo dovrebbe essere più breve di una normale valutazione a causa del tempo guadagnato durante la revisione progressiva.
Come dovrebbe agire il vaccino? Si prevede che BNT162b2 agisca preparando l'organismo a difendersi dall'infezione con il coronavirus SARS-CoV-2. Il virus utilizza proteine sulla sua superficie esterna, chiamate proteine spike, per entrare nelle cellule del corpo e causare malattie. BNT162b2 contiene le istruzioni genetiche (mRNA) per la proteina spike ed è ricoperto da piccoli grassi (particelle lipidiche) che impediscono la degradazione dell'mRNA.
Quando una persona riceve il vaccino, le sue cellule leggeranno le istruzioni genetiche e produrranno la proteina spike. Il sistema immunitario della persona tratterà quindi questa proteina come estranea e produrrà difese naturali - anticorpi e cellule T - contro di essa. Se, in seguito, la persona vaccinata entra in contatto con SARS-CoV-2, il sistema immunitario riconoscerà il virus e sarà pronto ad attaccarlo: anticorpi e cellule T possono lavorare insieme per uccidere il virus.
06 ottobre 2020
© Riproduzione riservata
Altri articoli in Scienza e Farmaci
gli speciali
Quotidianosanità.it
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Direttore responsabile
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Tel. (+39) 06.89.27.28.41
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
- Joint Venture
- SICS srl
- Edizioni
Health Communication srl
Copyright 2013 © QS Edizioni srl. Tutti i diritti sono riservati
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy