Quotidiano on line
di informazione sanitaria
Giovedì 02 MAGGIO 2024
Scienza e Farmacidi informazione sanitaria
Giovedì 02 MAGGIO 2024
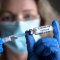
Farmaci. L’Ema ‘tira le somme’ del 2023: autorizzati 77 nuovi medicinali e 2 vaccini
Fra i prodotti autorizzati, 39 contenevano una nuova sostanza attiva che non era mai stata autorizzata prima nell'Unione europea (UE). Tra questi ci sono una serie di farmaci che si distinguono per il loro contributo nel rispondere ai bisogni di salute pubblica o per l’innovazione che rappresentano, rileva l’Agenzia
16 GEN - Nel 2023, l’Agenzia europea dei medicinali (Ema) ha raccomandato l’autorizzazione all’immissione in commercio per 77 medicinali. Di questi, 39 contenevano una nuova sostanza attiva che non era mai stata autorizzata prima nell'Unione europea (UE). Tra questi ci sono una serie di farmaci che si distinguono per il loro contributo nel rispondere ai bisogni di salute pubblica o per l’innovazione che rappresentano. E' quanto emerge da un documento di sintesi dell'attività annuale dell'Ema.L’Agenzia ha raccomandato due vaccini per la protezione contro la malattia del tratto respiratorio inferiore causata dal virus respiratorio sinciziale (RSV) e il primo medicinale per terapia avanzata che utilizza una tecnologia innovativa di modifica genetica nota come CRISPR/Cas9 per trattare due rare malattie del sangue. L’EMA ha inoltre adottato due pareri positivi per medicinali destinati all’uso in paesi al di fuori dell’UE. La panoramica delle raccomandazioni chiave per il 2023 pubblicata oggi comprende dati sull’autorizzazione dei medicinali e una selezione di nuovi trattamenti che rappresentano progressi significativi nelle rispettive aree terapeutiche. Una volta che un medicinale è autorizzato dalla Commissione europea e prescritto ai pazienti, l’EMA e gli Stati membri dell’UE ne monitorano continuamente la qualità e il rapporto rischi/benefici - ricorda l'Ema - e adottano misure normative quando necessario. Le misure possono includere una modifica alle informazioni sul prodotto, la sospensione o il ritiro di un medicinale o il ritiro di un numero limitato di lotti. Nel documento è inclusa anche una panoramica di alcune delle più importanti raccomandazioni relative alla sicurezza.
16 gennaio 2024
© Riproduzione riservata
Altri articoli in Scienza e Farmaci
gli speciali
Quotidianosanità.it
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Quotidiano online
d'informazione sanitaria.
QS Edizioni srl
P.I. 12298601001
Sede legale:
Via Giacomo Peroni, 400
00131 - Roma
Sede operativa:
Via della Stelletta, 23
00186 - Roma
Direttore responsabile
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Luciano Fassari
Direttore editoriale
Francesco Maria Avitto
Tel. (+39) 06.89.27.28.41
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
info@qsedizioni.it
redazione@qsedizioni.it
Coordinamento Pubblicità
commerciale@qsedizioni.it
- Joint Venture
- SICS srl
- Edizioni
Health Communication srl
Copyright 2013 © QS Edizioni srl. Tutti i diritti sono riservati
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy
- P.I. 12298601001
- iscrizione al ROC n. 23387
- iscrizione Tribunale di Roma n. 115/3013 del 22/05/2013
Riproduzione riservata.
Policy privacy