Omeopatici. Da Aifa le Domande e Risposte per presentazione domande di rinnovo dell’AIC

30 Gennaio 2017
© Riproduzione riservata
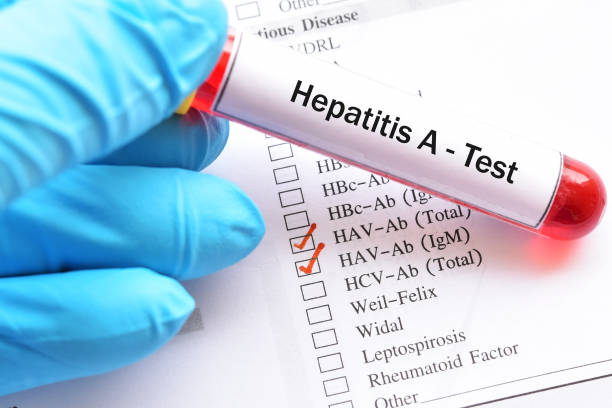
Crescono i casi di epatite A, sia per trasmissione sessuale che per alimenti contaminati
Crescono in Italia, analogamente a quanto avviene nel resto d’Europa, le segnalazioni di casi di epatite A, legati sia alla trasmissione sessuale che al consumo di prodotti contaminati. Lo segnala...
Alzheimer e demenze: in Italia 1 milione di pazienti, previsto raddoppio entro il 2050. Serve fare rete
In un paese come l’Italia, in cui il 23% della popolazione ha più di 65 anni con una speranza di vita sempre in aumento, l’Alzheimer rappresenta più che mai una...
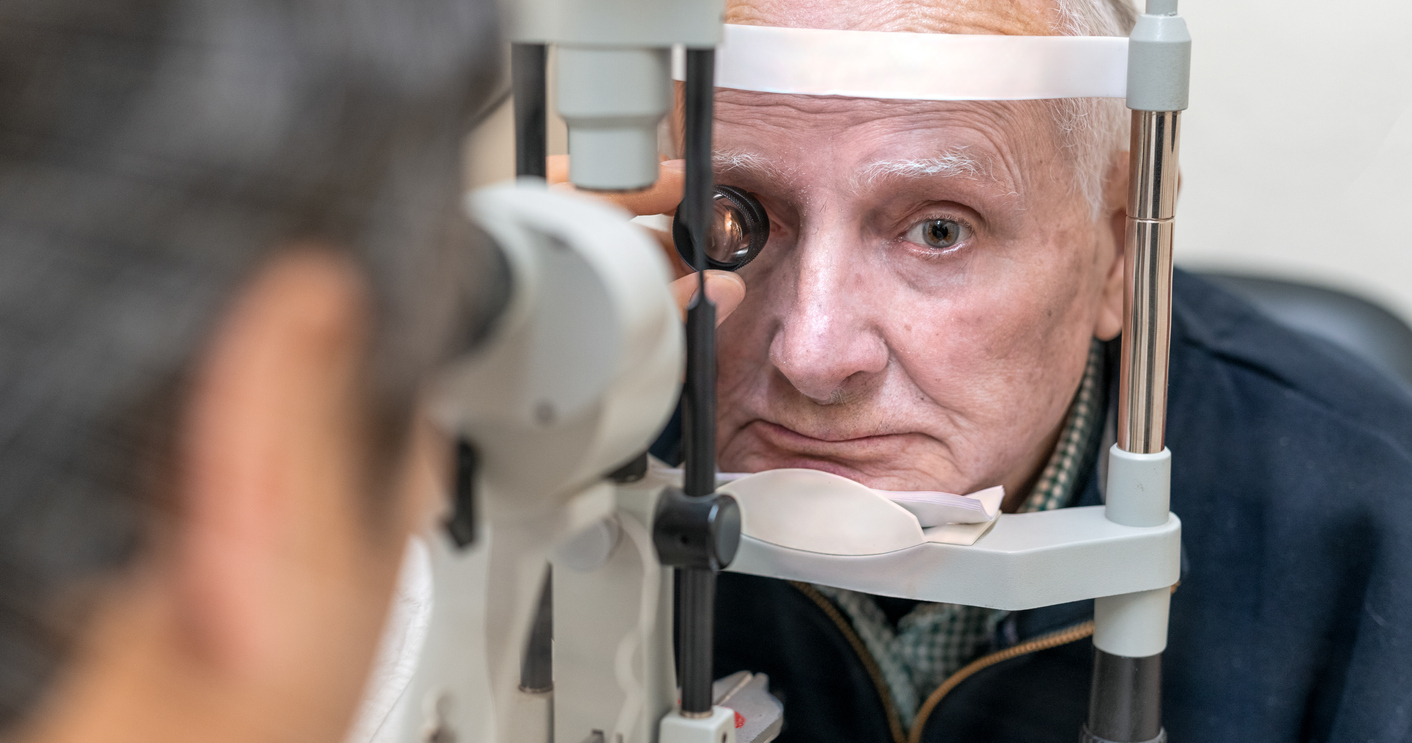
AIFA approva faricimab in siringa preriempita: un passo avanti per contrastare le principali patologie della retina
L’Agenzia Italiana del Farmaco (AIFA) ha approvato la rimborsabilità a carico del SSN per la nuova formulazione di faricimab in siringa preriempita (PFS), da utilizzare nel trattamento della degenerazione maculare...
Hiv. Simit: “In Italia i nuovi casi restano stabili, allontanandoci dagli obiettivi Unaids 2030”
Alla vigilia della Giornata Mondiale contro l’Aids del 1° dicembre, sotto i riflettori l’ultimo bollettino del Centro Operativo Aids dell’Istituto Superiore di Sanità, che nel 2024 registra 2.379 nuove diagnosi...