Quando e quale test effettuare per verificare la presenza di SARS-CoV-2? A fare ordine sono il Ministero della Salute e l’Istituto superiore di sanità che hanno appena pubblicato una nuova guida che delinea le strategie ottimali. Tra le indicazioni quella che il Test molecolare è da preferire in presenza di un caso sospetto sintomatico mentre il test rapido può essere la prima scelta per un contatto stretto di caso confermato. Test invece non raccomandato per i contatti di contatti stretti di caso confermato.
La sintesi del documento
Casi sospetti e casi positivi
– Il test è mirato alla ricerca del virus nel contesto delle indagini cliniche ed epidemiologiche di soggetti con sintomatologia compatibile con una infezione da SARS-CoV-2, inclusi i contatti stretti sintomatici, e ai test effettuati per definire la guarigione dei casi positivi.
Contatti stretti asintomatici
– I test devono essere limitati ai contatti stretti di un caso confermato sia che il test sia prescritto all’inizio che alla fine della quarantena di 10 giorni. A tal proposito si faccia riferimento alla circolare del Ministero della Salute n. 32850 del 12 ottobre 2020 “COVID-19: indicazioni per la durata ed il termine dell’isolamento e della quarantena”.
– Non è raccomandato prescrivere test diagnostici a contatti di contatti stretti di caso confermato; qualora essi vengano richiesti in autonomia, i soggetti non devono essere considerati sospetti né essere sottoposti ad alcuna misura di quarantena né segnalati al Dipartimento di Prevenzione tranne i positivi che vanno sempre comunicati.
– Se la richiesta dei test diagnostici, anche in ambito scolastico, per i contatti stretti, viene effettuata dal PLS/MMG, deve essere sempre accompagnata dalla segnalazione al Dipartimento di Prevenzione di competenza. Allo stesso tempo deve essere raccomandato al soggetto di rispettare l’isolamento domiciliare in attesa del risultato del test.
Indicazioni e considerazioni generali
– L’analisi diagnostica può essere effettuata solo presso laboratori, altamente specializzati, di riferimento regionali e laboratori aggiuntivi individuati dalle Regioni secondo le modalità e le procedure concordate con il Laboratorio di Riferimento Nazionale dell’Istituto Superiore di Sanità.
– I dati relativi ai test da qualsiasi soggetto vengano eseguiti devono essere riportati al Dipartimento di Prevenzione (DdP) per evitare ripetizioni di test e soprattutto un allineamento tra risultati dei test e azioni di sanità pubblica da parte del DdP.
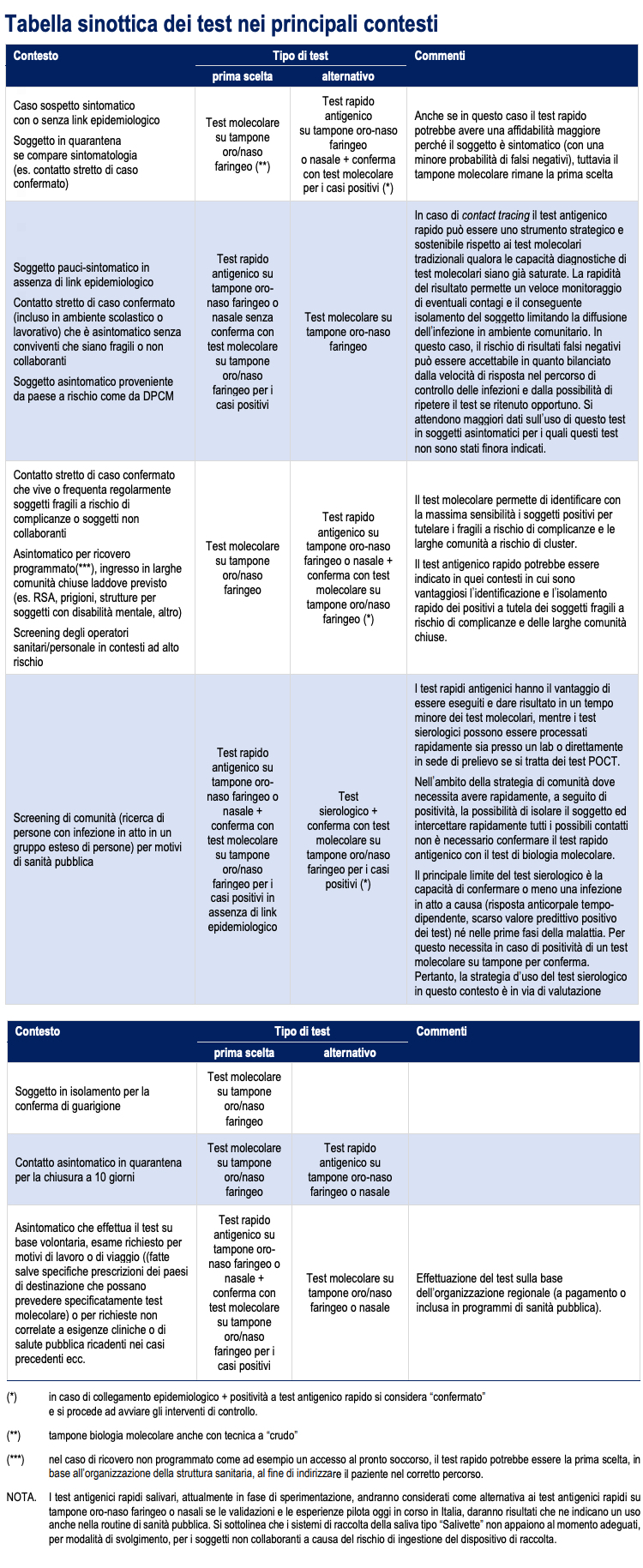
– La persona in attesa del risultato del test deve essere posta in quarantena. Se il risultato del test è positivo il DdP prescriverà l’isolamento alla persona interessata e la quarantena ai contatti stretti. Sebbene i test molecolari siano quelli di riferimento per sensibilità e specificità, in molte circostanze si può ricorrere ai test antigenici rapidi che, oltre essere meno laboriosi e costosi, possono fornire i risultati in meno di mezz’ora e sono eseguibili anche in modo delocalizzato e consentono se c’è link epidemiologico di accelerare le misure previste; per maggiori dettagli si veda la tabella sinottica allegata.
– Nei punti di esecuzione dei test (inclusi i drive-in) va definito un accesso prioritario per i test diagnostici prescritti ai soggetti sintomatici e ai contatti stretti asintomatici di un caso confermato e alle altre categorie previste. L’esecuzione di test non prioritari potrebbe essere organizzata in altri contesti separati e con altre modalità per evitare di allungare i tempi di prelievo (ad esempio presso laboratori accreditati) e di risposta del risultato essenziali per le successive indagini cliniche e per azioni di sanità pubblica.
– Nel caso di test antigenici rapidi si suggerisce un adeguato approvvigionamento di strumentazione per la lettura dei tamponi al fine di ottimizzare la capacità di fornire risultati in meno di 30 minuti direttamente sul luogo di prelievo. La strumentazione viene fornita insieme ai test per quelli che usano la fluorescenza (FIA) o altri sistemi strumentali mentre i test immunocromatografici non necessitano di lettori.
– Alla luce del previsto diffuso uso del test antigenici rapidi e della loro semplicità di esecuzione, è ipotizzabile attuare un coinvolgimento della rete dei pediatri di libera scelta e del medico di medicina generale per l’uso nei diversi contesti organizzativi, incluso quello delle indagini di comunità, fermo restando la necessità di garantire le misure organizzative, di prevenzione e protezione adeguate.
– Allo stato attuale i test rapidi salivari (antigenici o molecolari) sono in fase di valutazione anche in contesti territoriali. Le attuali esperienze pilota permetteranno raccogliere dati utili per definire le loro indicazioni di utilizzo nel prossimo futuro.
– Si rappresenta che la definizione di “caso confermato” dovrebbe essere aggiornata in relazione all’utilizzo dei test antigenici rapidi senza una conferma con test molecolari soprattutto in presenza di situazioni con link epidemiologico dove la positività del test rapido individua di per sé l’intervento come “caso”, per l’attivazione rapida delle azioni di controllo.
– È importante la condivisione dei dati a livello locale/regionale/nazionale delle validazioni su vari tipi di test antigenici rapidi, inclusi quelli salivari, in commercio nel nostro paese per ottimizzare le strategie del loro uso.
– Si sottolinea che l’evoluzione delle diverse tipologie dei test è continua e che ai fini della loro valutazione possono essere considerate affidabili le validazioni effettuate dalle agenzie regolatorie dei Paesi del G7.